脱硫废水处理系统产生的污泥既具有良好的吸附性能,又具有钙盐除磷的作用,且同时污泥自身的高碱度有助于化学吸附除磷。因此,研究脱硫废水处理系统污泥资源化除磷技术具有实用价值和环保意义。
1、实验材料与实验内容
1.1 实验材料
(1)脱硫污泥。
取3份某电厂脱硫废水,投加CaO分别调节pH值至9、10和11,在实验室模拟反应池中充分反应,再投加絮凝剂使污泥颗粒聚集成团,于实验室模拟沉淀池中进行泥水分离。将污泥于50℃下烘干,研磨,过100目细筛(筛孔孔径为0.149mm)后收集待用,分别标记为S9、S10和S11。根据溶固反应测定,3种污泥的钙质量分数分别为0.0732、0.0819和0.0944。
(2)模拟含磷废水。
用NaH2PO4配制高含磷废水,初始磷(以P计)质量浓度为55mg/L。
1.2 实验内容
(1)除磷实验。分别投加污泥样品S9、S10和S11于200mL模拟含磷废水中,在100r/min条件下搅拌120min,沉降30min,取上清液测定pH值和PO43−浓度(以P计),计算P去除率(PRE)。
(2)动力学实验。
取3份500mL模拟含磷废水,分别投加3种污泥样品进行除磷实验,在120min内间隔取水样(过滤),测定PO43−浓度(以P计),用以拟合动力学方程。
(3)热力学实验。
考虑不同季节水温变化,选择在25℃、30℃和35℃条件下进行热力学实验研究,分别在不同操作温度下,将模拟含磷废水置于摇床中进行除磷实验,振荡条件为200r/min,24h后,取上清液测定PO43−浓度(以P计),用以拟合热力学方程。
2、实验结果与讨论
2.1 脱硫废水水质特点
某电厂脱硫废水原水和“三联箱”工艺出水水质如表1所示。脱硫废水中含有高浓度固体悬浮物(SS)、Ca2+、Mg2+和Cl-,以及少量重金属,经“三联箱”工艺处理后,水中SS下降90%以上,重金属Cd2+、As3+和Mn2+的去除率在99%以上,Hg2+的去除率达85%,残余量均小于《污水排放标准》的要求值。一般情况下,“三联箱”工艺出水回用至排渣系统。由于工艺中需投加CaO,使钙质量浓度增加值为300mg/L,而出水中Ca2+质量浓度仅增加128mg/L,说明污泥中含有丰富的钙盐。含钙污泥投加到含磷废水中,钙与磷会发生化学反应,从而起到化学除磷作用。
2.2 不同污泥浓度及含钙量对磷去除率的影响
为了研究污泥含钙量对除磷过程的影响,选择含钙量不同的3种污泥样品(S9、S10和S11)进行除磷实验。在碱性条件下,污泥中的钙与模拟废水中的磷可发生反应,试验结果如图1所示。由图1可知,3种污泥的P去除率随污泥投加浓度的增大均呈现先迅速增大随后平缓增加的趋势,对应的变化趋势拐点分别在投加S9、S10、S11污泥质量浓度为10g/L、2.5g/L、2g/L时,当投加S9、S10、S11污泥质量浓度分别增加到30g/L、4g/L、3g/L时,P去除率均可达99%以上。可见3种污泥均能达到较彻底的除磷效果,含钙量高的污泥用量显著减少。经测试,S9、S10和S11的粒径分别为30.82μm、29.12μm和25.24μm,比表面积分别为7.52m2/g、7.89m2/g和8.25m2/g,说明含钙量高的污泥粒径更小,比表面积更大,具有更强的吸附能力。
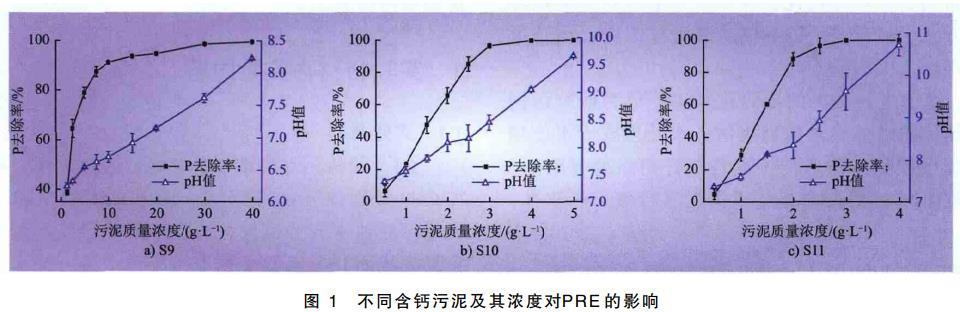
由图1还可看出,模拟含磷废水pH值呈现先缓慢增大后迅速增加的趋势,这是因为3种污泥自身均为碱性,随污泥投加量的增加,会提高水溶液的pH值。当P去除率达90%~100%时,废水pH值均在7.0~10.0范围内,该pH值条件下磷主要以H2PO4−和HPO42−形式存在,反应产物为CaHPO4·2H2O沉淀。由于CaHPO4·2H2O为微溶物,在25℃时溶解度为4.303×10−2g/L,完全反应时水中P的浓度为7.76mg/L,即化学除磷的P去除率仅为86%,而3种污泥样品的除磷实验结果表明,当污泥浓度达到一定范围时,均可使P去除率大于99%。由此可见,含钙污泥除磷是化学反应和吸附作用的共同结果。当污泥浓度较低时,污泥除磷受化学反应控制,反应过程中消耗一定量OH−,pH值变化平缓,随着污泥浓度的增加,反应至终点,pH值直线上升,污泥吸附占主导作用,直到P去除率接近100%。由于污泥表面Ca2+对水中HPO42−存在化学吸附作用,污泥含钙量越高,对磷的吸附容量越大,越有利于吸附除磷。
通过以上试验得到:S9、S10和S11除磷适宜的质量浓度范围分别为1.0~40g/L、0.5~5.0g/L、0.5~4.0g/L。
2.3 吸附动力学
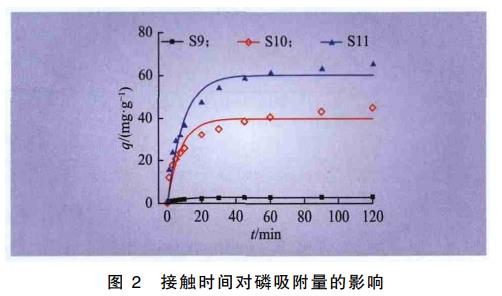
根据2.2中除磷实验结果可知,S9、S10、S11质量浓度分别为10g/L、2.5g/L、2g/L时,污泥吸附作用占主导,因此选取该污泥浓度进行动力学和热力学实验,研究除磷机制。不同接触时间3种污泥对磷的吸附量(q,单位质量吸附剂(g)吸附P的质量(mg),以mg/g表示)如图2所示。由图2可见,在吸附开始阶段,3种污泥对磷的吸附量均迅速增加,前20min属于快速吸附阶段,随后缓慢增加,在45min时均达到吸附平衡。相同接触时间内S11对磷的吸附量最大,且吸附速度最快,这与2.2中除磷实验结果一致。
为了分析3种污泥对磷的吸附机理,采用拟一级动力学模型(式(1))、拟二级动力学模型(式(2))和粒子内扩散模型(式(3))对实验数据进行拟合。
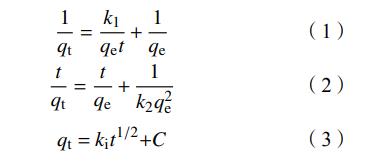
式中:与分别为t时间与吸附平衡时单位质量吸附剂(g)吸附P的质量(mg),mg/g,k1为拟一级速率常数,min-1,k2为拟二级速率常数,g/(mg·min),k1为粒子内扩散速率常数,mg/(g·min1/2),C与边界层的厚度有关。
根据式(1)、(2)、(3)得到的拟合结果,分别如图3a)、b)和c)所示,所得可决系数(R2)、平衡吸附量qe和速率常数(k1、k2、ki)如表2所示。由表2可知,拟二级动力学模型的R2均高于0.994,表明污泥对磷的吸附过程更符合拟二级动力学模型,吸附作用是速率控制步骤[15-16]。S10和S11的平衡吸附容量是S9的15~22倍,因此污泥S10和S11通过吸附作用除磷所需污泥量远小于S9,与前述除磷实验结果相符。
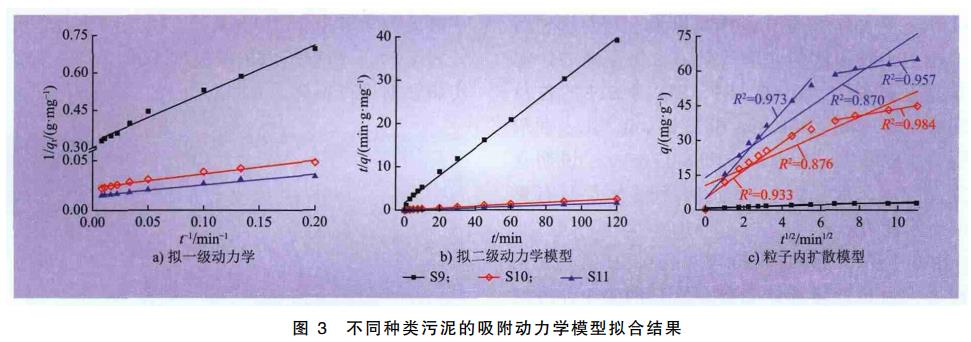
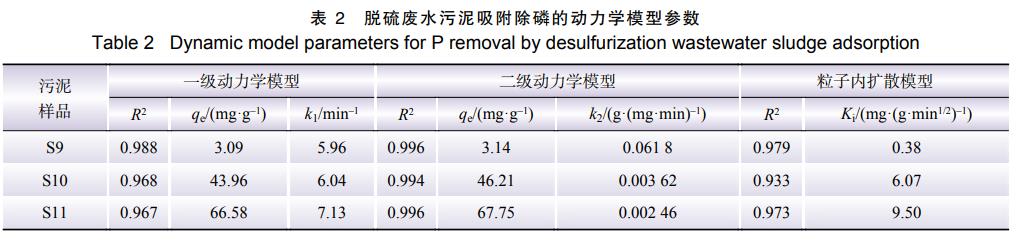
采用粒子内扩散模型拟合吸附实验数据,研究污泥对磷的吸附动力学机理,结果如图3c)所示。吸附过程包含2个阶段,第1阶段为外部传质或者膜扩散过程,其直线不过零点,即可假设粒子内扩散是控制吸附过程的限速步骤,同时该过程还受膜扩散的联合控制,第2阶段为吸附平衡阶段,此时粒子内扩散速度减慢,原因为经快速吸附阶段后溶液中磷浓度较低。综合上述结果,可以推测:在初始吸附阶段,废水中的磷与污泥充分接触,而后发生反应,磷主要被污泥表面的钙所吸附,而不是扩散至污泥孔内发生反应。
2.4 吸附热力学
分别采用Langmuir模型(式(4))和Freundlich模型((式5))拟合3种污泥在不同温度下的吸附等温线。

25℃、30℃和35℃下3种污泥的Langmuir和Freundlich吸附曲线拟合参数及结果分别如表3和表4所示。
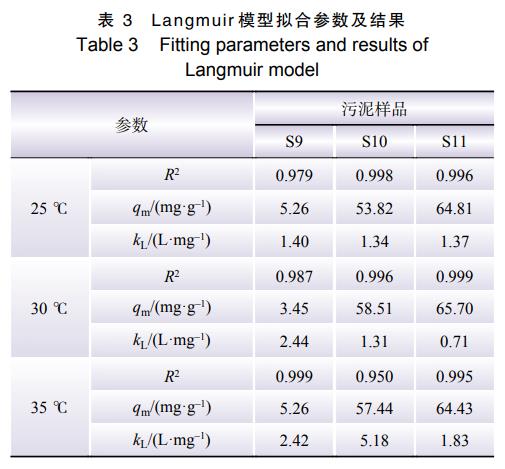
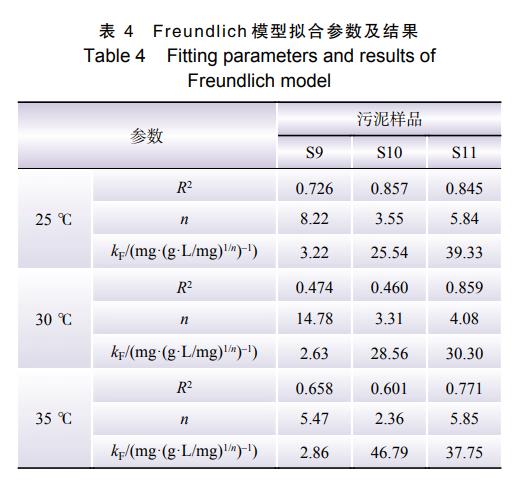
由表3、4可知,Langmuir吸附等温线的R2均大于0.950,明显高于Freundlich模型,因此污泥对磷的吸附平衡过程更符合Langmuir吸附等温线。如表3所示,3种污泥的饱和吸附量均随着温度升高而增加,即适当升温对污泥吸附磷有促进作用。Langmuir吸附过程为单层吸附,这意味着磷的吸附去除发生在污泥表面,这与实验结论相一致。kL表示吸附能力的强度,且kL大于0,说明污泥对磷的吸附作用为有利吸附[18]。综上所述,污泥吸附除磷即为污泥表面的钙对废水中磷的吸附,吸附过程只发生在污泥表面。
2.5 污泥的XRD和SEM分析
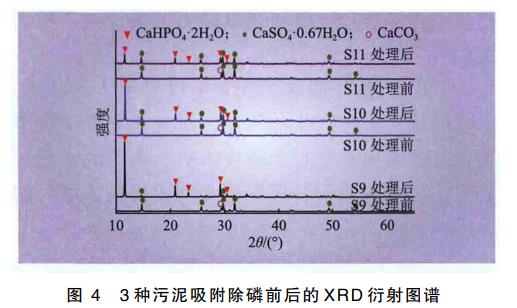
对吸附前后的污泥进行XRD和SEM分析,结果如图4和图5所示。由图4可见,3种污泥吸附前的XRD图谱均在14.7°、29.7°和31.9°处有3个强峰,在25.6°和49.4°处有2个次峰和1个弱峰,表明吸附前的污泥主相为CaSO4·0.67H2O,同时在29.4°处有1个CaCO3的特征峰。吸附后的XRD图谱均在11.7°处有1个强峰,在20.9°和29.3°处有2个次峰和2个弱峰,表明吸附后的污泥表面有透钙磷石(CaHPO4·2H2O)生成,进一步验证了前述结论。

由图5可见,吸附前的3种污泥表面较为平整,结构相近,而吸附后的污泥表面出现团聚的花瓣状晶体,其为透钙磷石的典型结构,这一形貌变化证明污泥表面已发生化学吸附,大量透磷钙石覆盖在污泥表面。相对于S9而言,S10的花瓣状晶体结构较为松散,但数量增大,S11则较S10结构紧密,即污泥表面透磷钙石更多,说明其对磷的吸附作用更强。
3、结论与展望
(1)脱硫废水处理系统所产生的含钙污泥,具有高效吸附除磷的作用。提高污泥含钙量和污泥浓度均能达到较彻底的除磷效果,其中含钙量的影响更加显著,除磷过程是化学反应和化学吸附的共同结果。
(2)动力学和热力学研究表明,该吸附过程为污泥表面的单层化学吸附,内扩散和膜扩散共同控制吸附速率。XRD和SEM分析表明,吸附过程中污泥表面会形成透钙磷石,未发现磷酸钙沉淀。
(3)为防止脱硫污泥重金属对水体的污染,“三联箱”工艺产生的污泥,可先作为除磷吸附剂,经济高效地处理含磷废水后,再经脱水另行处置。这种方式为污泥资源化利用提供了可行的手段。(>
如需要产品及技术服务,请拨打服务热线:13659219533
选择太阳集团城娱8722,你永远值得信赖的产品!
了解更多,请点击www.botaida.com







